O Paradoxo do cristal

E por isso Shechtman tinham mais satisfação do que o comum quando subiu ao palco, em Estocolmo, em dezembro do ano passado, para receber o Nobel de química. Ele foi ousado – e estava certo.
No começo dos anos 80, Shechtman estava atirando raios de elétrons em misturas de metais. Ele analisou os padrões de interferência, permitindo que determinasse o formato dos átomos internos.
Um padrão de interferência nitidamente definido é sinal de uma estrutura cristalina regular. Mas entre as misturas que ele estudou, um lindo padrão formado pelo alumínio e o manganês não fez sentido. Ele sugeria um cristal com uma simetria do pentágono. Mas as leis dos cristais diziam que os átomos não podem estar arranjados dessa maneira, assim como pentágonos não podem preencher um piso sem deixar buracos.
Pauling não era o único cético na história. Quando Shechtman insistiu na sua ideia, ele foi convidado a se retirar do grupo de pesquisa e teve muita dificuldade em conseguir publicar suas descobertas.
De fato, a resposta para a discussão estava lá. Na década de 70, o matemático Roger Penrose descobriu que dois azulejos no formato de diamantes podiam cobrir um plano sem deixar buracos e sem repetir o padrão. O padrão dos átomos de Shechtman nunca se repetia exatamente, e por isso não formava um cristal perfeito; era um “quasicristal”.
Desde então, muitos outros cristais desse tipo foram encontrados. Estruturas similares estão em vários polímeros e até em um fragmento de um meteorito encontrado na Sibéria. Em 2010, uma equipe liderada por Valeria Molinero até sugeriu que a água, quando confinada em pequenas aberturas, pode congelar e formar um gelo quasicristal.
Entropia em ambas
as direções

Pelo menos ele viveu o suficiente para ver o desprezo dado ao seu trabalho virar uma grande aceitação. Na década de 50, Boris inventou um coquetel de ingredientes químicos que conseguia imitar a glicólise, o processo pelo qual as enzimas quebram os açucares. A mistura passava de incolor para amarela conforme a reação acontecia.
Mas então algo incrível ocorreu: o coquetel ficou incolor novamente. E depois amarelo. E depois incolor. Passou a oscilar repetidamente entre os dois estados.
Isso era inaceitável. Uma reação que fosse espontaneamente para ambas as direções ia contra um dos ditos mais sagrados da química, a segunda lei da termodinâmica. As mudanças de estado no universo são acompanhadas de entropia – em outras palavras, é preciso deixar as coisas menos ordenadas do que estavam antes. A entropia não pode aumentar em ambas as direções em uma reação química. Belousov estava sugerindo algo insano.
De fato, Belousov não foi o primeiro a observer o evento. Em 1921, o químico americano William Bray confirmou oscilações similares quando o peróxido de hidrogênio regia com íons iodados. Mas ninguém acreditou nele, também. E Belousov não conseguia publicar sua descoberta.
A fama só veio quando o compatriota Anatoly Zhabotinsky modificou a reação original para revezar as cores do azul para o vermelho – uma mudança muito drástica para ser ignorada. Conforme as novidades da reação “Belousov-Zhabotinsky” (BZ) viajavam para o ocidente, no fim da década de 60, uma explicação começou a se cristalizar. As oscilações acontecem porque a reação inicial gera componentes intermediários que são auto catalíticos, aumentando sua própria produção. Ao mesmo tempo, alguns dos componentes resultantes iniciam um segundo ciclo autocatalítico que regenera os ingredientes do primeiro.
Mas as oscilações não duram para sempre: se deixadas, lentamente elas param, e a mistura fica em um estado imutável. Elas são um exemplo de um fenômeno transitório sem equilíbrio. A termodinâmica lida apenas com estados equilibrados, por isso a segunda lei não está ameaçada.
Mas se a reação BZ for constantemente alimentada com ingredientes frescos, e os produtos finais forem removidos, as oscilações continuam indefinidamente. Esse processo é importante para algumas reações industriais e até mesmo na glicólise real.
Túnel de escape quântico

A maior parte das reações químicas procede através da formação de moléculas intermediárias de alta energia, que se arranjam para formar produtos de menor energia. Geralmente na forma de calor, a energia é necessária para cruzar a barreira dos reagentes. De acordo com a teoria “cinética” padrão, quase todas as moléculas nas frígidas nuvens de gás interestelares não teriam energia suficiente para reagir.
Na década de 70, o cientista soviético Vitali Goldanski desafiou esse dogma. Seus experimentos mostraram que certas moléculas envolvidas em reações de polímeros continuavam a acontecer mesmo quando resfriadas até menos 269,15 graus Celsius, um pouco mais quente do que as partes mais frias do espaço. O formaldeído, um componente comum nas nuvens moleculares, pode se unir em cadeias de polímeros com centenas de moléculas, usando uma ajuda de raios gama ou elétrons energizados – elementos que estão viajando pelo universo.
Como isso era possível? Goldanski argumentou que a ideia convencional estava esquecendo um elemento crucial. As leis quânticas ditam que partículas como os átomos e os elétrons envolvidos em reações químicas podem cruzar as barreiras energéticas, mesmo que aparentemente não haja energia suficiente. Isso acontece através de um processo chamado “túnel”. O cientista disse que no frio espaço, esse processo de canalização mantém as coisas acontecendo.
O trabalho de Goldanski foi uma curiosidade na época, mas o princípio quântico hoje está bem estabilizado. Algumas reações biológicas, catalisadas por enzimas, são mais eficientes do que a teoria cinética porque envolvem o movimento de íons de hidrogênio – prótons solitários que são mais inclinados ao túnel quântico.
Mas ainda assim podem acontecer surpresas. Em junho do ano passado, Wesley Allen e seus colegas prenderam uma molécula super reativa, livre de radicais, chamada de metilhidroxicarbono em uma matriz de argônio sólido, a menos 262,15 graus Celsius. Ela tem elétrons sem par que são predispostos a reagir rapidamente – mas não a essas temperaturas.
Não apenas a molécula reagiu, mas também formou o produto errado. A molécula pode se rearranjar para formar ou acetaldeído ou álcool vinil, mas a barreira energética para o segundo é menor, então mais dele é esperado. Ao invés disso, formou-se uma quantidade muito grande de acetaldeído.
Allen propõe que apesar da barreira para formar o acetaldeído ser maior, ela é também mais curta, tornando o processo do túnel mais fácil. Ele afirma que isso “foi um choque para a maioria dos químicos”.
Forçando os gases nobres
a trabalhar

A história desses elementos, empilhados à direita na tabela periódica, dá amplo suporte para essa visão. Após a descoberta do gás argônio, em 1894, o químico francês Henri Moissan o misturou com flúor, o elemento reativo que ele havia isolado em 1886, junto com faíscas para uma boa mistura. Resultado: nada.
A teoria das ligações químicas explicava o porquê. Os gases nobres estão cheios de elétrons, então não podem compartilhar com outros átomos.
O influente químico Linus Pauling foi um dos maiores arquitetos dessa teoria, mas sem desistir imediatamente dos gases nobres. Na década de 30, ele conseguiu uma rara amostra de xenônio e convenceu seu colega Don Yosta a tentar reagir com o flúor. Após muita tentativa, Yost conseguiu apenas corroer as bordas do frasco de quartzo.
Após isso, só um louco iria querer fazer compostos de gases nobres.
O químico inglês Neil Bartlett não tentou contrariar a sabedoria convencional; só começou a seguir a lógica comum. Em 1961, ele descobriu que o composto de platina hexafluorida (PtF6), formado três anos antes, era um poderoso oxidante. A oxidação, que remove elétrons de um elemento ou composto químico, leva o nome do oxigênio porque ele é incomparável nessa função. Mas Bartlett descobriu que a PtF6 podia oxidar o oxigênio, arrancando os elétrons e criando um íon positivo.
No começo do ano seguinte, Barlett estava preparando uma aula e viu um gráfico de “potências de ionização”. Esses números contam a quantidade de energia necessária para remover um elétron de várias substâncias. Ele percebeu que o potencial de ionização do xenônio era quase igual ao do oxigênio. Se a PtF6 podia oxidar o oxigênio, que tal o xenônio?
A mistura do gás vermelho de PtF6 e o xenônio incolor respondeu a questão. O vidro imediatamente ficou coberto por um material amarelo. A fórmula do composto formado era XePtF6, o primeiro composto de gases nobres.
Muitos outros foram formados depois. Alguns são muito instáveis: Bartlett quase perdeu um olho estudando o dióxido de xenônio. Mesmo hoje, os gases nobres continuam a surpreender. O ganhador do Nobel, Roald Hoffmann, admite ter ficado chocado quando soube que, em 2000, químicos de Berlim formaram um composto de xenônio e ouro – um metal que é supostamente nobre e não reativo.
Então não acredite em tudo que contam na escola. Os gases nobres continuam sendo os elementos menos reativos por aí, mas parece que você pode fazer de tudo com a química.
Ménage à trois atômico
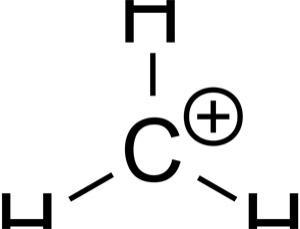
Tudo começou nos anos 40, com tentativas de explicar certas reações de moléculas orgânicas que envolviam a mudança de grupos carregados negativamente. Se um desses grupos sumia, sobrava um íon contendo um átomo de carbono carregado positivamente. De acordo com as teorias, o grupo de substituição deveria se ligar no mesmo lugar, no átomo positivo. Mas isso não acontece sempre.
Alguns químicos, em particular Saul Winstein, deram uma surpreendente afirmação: que a carga positiva estava rodeada em um arranjo triangular, com três carbonos.
NewScientist



